摘要
重力,是心血管最早的老師,也是最長久的訓練場
站立、行走,這種在平常不過的姿勢和運動,在重力的影響下,對於人類的心血管系統卻是一項巨大的挑戰。
心臟位於左胸,高於人體大約 75% 的血液。
當我們由平躺轉為站立時,沿垂直方向作用的靜水壓會使腿部與下半身靜脈血液暫時「沉積」,估計約有 500–1000 毫升的血液滯留在下肢與腹部,返回心臟的血液量因而減少,這會觸發複雜的反射反應,以維持血液流向大腦。
上半身動、靜脈的壓力和體積減少,會導致交感神經活性增加,心跳強度和速度上升、血管收縮,同時啟動腎素–血管張力素–醛固酮系統以及抗利尿激素等內分泌反應,以維持血壓與循環血容量(blood volume)。
站立時血壓調節的關鍵刺激是頸動脈竇與主動脈弓壓力受器的牽張與放電減少,而非單純上半身血管容量減少。
這些演化而來的生理機制,幫助人類適應地球的重力環境。
也就是,為了讓血液仍能順利送到大腦,身體會立即啟動壓力反射,包括交感活性增加、心跳加快、血管收縮,並透過 RAAS 與抗利尿激素調節血容量。這些機制,都是人類在地球重力下長久演化出的「心血管維生法則」。
當靜水壓突然消失:1–2 公升的血往上跑,心血管規則被重寫
然而,當進入太空的失重環境時,重力引起的靜水壓力梯度消失,體液在體內重新分布,約有 1–2 公升血液和組織液自下半身和腹部向頭胸部移動(多數研究以約 1 公升為主,少數報告更高),這增加了身體上部的液體壓力,降低了身體下部的壓力,導致許多太空人都經歷過「浮腫臉」和「鳥腿」。
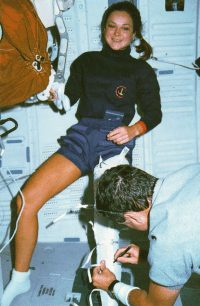
這不是單純的「臉變腫」而已,而是心臟與血管突然被迫在全新的物理規則下工作,這也是「太空醫學」中最經典、最基礎的一課。
在太空暫時適應,回地球卻難以承受:心血管「生理退化」的開始
當心臟和頸動脈竇壓力感受器檢測到頭胸部液體壓力和體積的增加,會啟動一連串反射反應,嘗試將血壓與血容量拉回到新的「平衡點」,包括利尿增加、交感活性與腎素–血管張力素–醛固酮系統被抑制等。
太空人會覺得自己在太空中很正常,卻沒察覺心臟與周邊血管正在重新調整配置,逐步喪失抵抗重力的能力。
這些反應讓太空人在失重環境下多半仍能正常活動,但心血管系統其實正逐步出現『生理退化』(deconditioning)。一旦返回有重力的環境,問題就會被放大顯現。
一旦太空人從失重狀態返回,靜水壓力梯度的恢復會再度將血液、體液和組織液向腳部拉動,心血管系統已經去條件化,無法立刻滿足這一新需求,於是便出現所謂的太空飛行失調(Spaceflight deconditioning),包含:體位不耐受(orthostatic intolerance)、心臟萎縮(cardiac atrophy)、血管功能障礙(vascular dysfunction)和工作能力損失等現象。
失重造成的生理變化:心臟與血管如何重新運作?
血漿量縮水:失重環境的第一個心血管代價
血漿容量的下降並非太空飛行者獨有,長期臥床者同樣會發生,只是過去常被誤以為兩者機轉完全不同。
它們共享一個核心特徵:頭胸部相對充血使壓力受器誤以為循環血容量偏高,因此抑制交感神經與腎素–血管張力素–醛固酮系統的活性,促進利尿,使血液量下降更為明顯。
差別在於,太空飛行是在完全失重的情況下進行,液體重分布的程度比臥床更劇烈,帶來更快速且更顯著的血漿量與總血液量減少,後期甚至還會伴隨骨骼肌量與紅血球生成的調整,使血液量下降更為明顯。
在失重狀態中,由於頭胸部血液增加,壓力感受器系統受到抑制,整體反射反應偏向「排出」而非「保留」血容量,於是利尿增加,使總血液量下降更為明顯。
同時,體液在體內的位置重新分布,部分水分會從血管移向組織間液,但真正影響心血管功能的,並非水分短暫跑到哪裡,而是整體「有效循環血容量」的降低 — 這使心臟前負荷下降,也成為後續心臟萎縮與姿勢不耐受的重要基礎。
此外,太空飛行初期紅血球生成素(EPO)分泌會短暫下降,使紅血球量在數天內即減少,並在前 10 天內出現約一成左右的紅血球質量下降,形成早期的「太空性貧血」(space anemia)。
周邊血管變「懶惰」:最先退化的是腿
太空飛行對於血管最明顯的影響,是周邊血管收縮能力的下降,而這也被認為是太空人返回地球後姿勢不耐受的重要原因之一。
研究顯示,在長期失重的情況下,腿部血管的內膜–中膜厚度(intima–media thickness)會減少,使內皮釋放的一氧化氮更容易擴散進入平滑肌,引發更強烈的血管舒張反應。
除了結構變化外,動物的模擬失重實驗亦發現,下半身動脈在長時間缺乏重力負荷的情況下,會出現功能性的重塑:平滑肌細胞的鉀離子通道開啟時間延長,使膜電位更容易過極化;同時,肌漿網釋放鈣離子的能力下降,使得平滑肌細胞在需要收縮時更不敏感。這些改變共同削弱了血管的基礎張力,使下肢血管在重力重新出現時,難以快速產生足夠的收縮來對抗血液往下肢沉降的趨勢。
腿部血管同時出現結構性與功能性退化,使恢復地面重力時血管無法即時產生足夠收縮。
相較之下,上半身血管因在失重期間承受較多液體負荷,調整方向可能與下半身相反,呈現不同的結構與功能適應。
整體而言,這些來自失重環境的結構與生理變化,使得返回地球後的血管更難有效調節血流分布,也是太空人著陸後容易頭暈與站立困難的背景因素。
心臟真的變小了:短短約十天即可看到萎縮
在地面上,心臟萎縮常發生於活動量降低或長期臥床者身上;但在太空中,造成心臟萎縮的因素更為複雜,包括血漿與總血液量的減少、靜水壓力梯度的完全消失,使前負荷降低,以及失重環境下整體運動量與心臟機械負荷下降等,最終使心臟逐漸出現萎縮的現象。
針對水星、雙子星、阿波羅與 Skylab 等任務的太空人研究發現,飛行前後的心胸比(最大水平心臟直徑與最大水平胸徑的比值)平均下降約 5%(下圖),顯示心臟尺寸在任務後確實縮小。
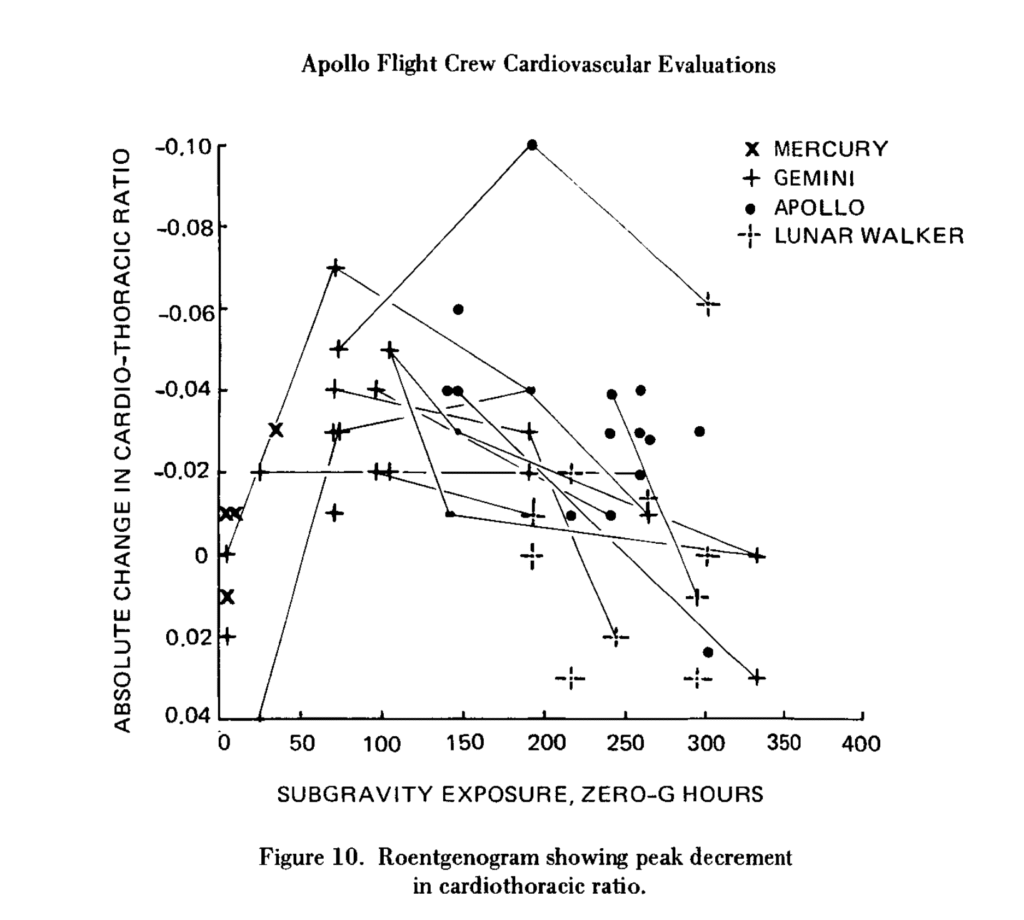
心臟在失重環境中處於『機械性去負荷』狀態(mechanical unloading),是造成心肌質量減少的核心原因。
心臟萎縮不僅僅影響心肌質量,也伴隨心室容積下降,推測與心室順應性減少、舒張期吸力(diastolic suction)降低有關,兩者都會使心動搏出量降低,進而成為姿勢不耐受的間接原因之一。
更值得注意的是,部分研究指出短短約十天的太空飛行,就足以觀察到明顯的心臟萎縮,而在返回地球後,心臟要恢復原有的尺寸與功能往往需要數倍於飛行時間的調適期,顯示心血管系統在失重下的退化速度遠比恢復速度快。
太空人最常遇到的心血管問題
回地球後站不起來:姿勢不耐受(OI)
姿勢不耐受(Orthostatic Intolerance, OI)是太空飛行後最具代表性的心血管問題之一,指的是在直立姿勢時無法維持足夠的血壓與心輸出量來供應腦部血流。
從太空計畫早期開始,著陸後發生 OI 就已是明確記錄的後果。太空人常在著陸後幾小時內出現心率加快、血壓下降、頭暈、視線模糊等暈厥前期症狀,甚至無法進行簡單的站立測試。
過去的數據顯示,約有五分之一的太空梭太空人無法忍受十分鐘的安靜直立,而在執行較長期任務(如國際太空站)後,暈厥前期症狀的發生率可大幅增加至超過六成。

儘管相關研究進行多年,OI 的確切機制仍未完全釐清,但普遍認為它是多重因素共同造成的,包括血漿容量減少使前負荷不足、下肢血管在失重期間喪失正常收縮能力、心臟萎縮導致心動搏出量變小,以及心室順應性降低等。
此外,失重期間壓力反射(baroreflex)與自主神經調節能力下降,也使太空人返地後更難快速應對重力突然恢復時的血壓變化。飛行時間長短與性別亦會影響 OI 的發生率,長期任務比短期任務更容易出現,女性太空人的發生率也較高。
失重期間會降低壓力反射敏感度(baroreflex sensitivity, BRS),使返地時無法快速調整血壓。
過往阿波羅與太空梭任務的太空人多能在三天內恢復直立反應,而 Skylab 與國際太空站等長期任務後,恢復時間則可能延長至一週甚至更久。雖然 OI 聽起來不至於危及生命,但若在飛行器意外著陸、缺乏地面支援的情況下發生,可能導致嚴重的後果。
未來登陸月球或火星的任務,也必須慎重評估這項風險。
運動能力下降:心臟輸出不夠、血管反應慢、體溫與乳酸紊亂
心血管系統負責將氧氣與營養素送往周邊組織,並回收代謝廢物,因此運動與工作能力本質上都取決於血流供應的效率。太空人在失重期間,新陳代謝的負荷比地表低,再加上血漿與總血液量下降、心臟前負荷減少、心臟萎縮與血管收縮能力變差,使得運動和工作能力普遍降低。
NASA 早期的研究顯示,可以透過次最大運動(submaximal exercise)時心率上升的幅度來推估最大運動能力或最大攝氧量的變化。
Skylab 與國際太空站的資料顯示,次最大運動心率在太空飛行初期常會出現些微上升,但真正明顯的變化往往是在返回地球後,心率比地面基線更高,且需要大約 30–45 天才能完全恢復。
雖然太空飛行會造成骨骼肌、骨骼、神經前庭等多系統退化,但就本篇主題而言,心血管系統的生理退化是太空任務能否安全完成的關鍵之一。
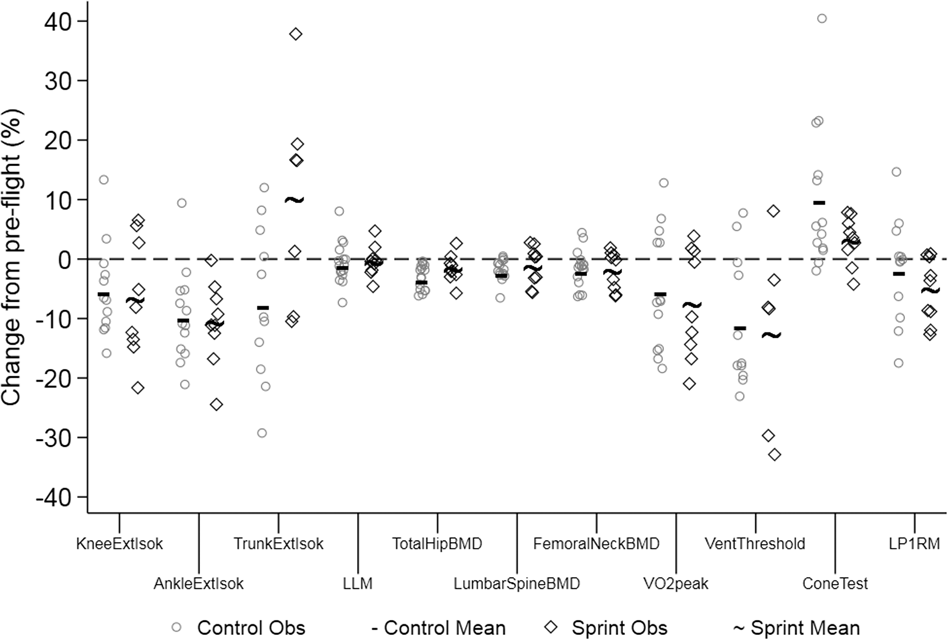
若比較太空梭與國際太空站兩類任務,太空梭太空人在任務期間的最大有氧能力多能維持在接近正常的範圍,而國際太空站的太空人則明顯下降。推測原因是 ISS 的工作負荷更高,早期進站後常無法立即投入完整訓練,使心血管去條件化更為明顯。
在恢復期方面,太空梭任務的太空人大約兩週後即可回到原有狀態,而 ISS 任務後則需要超過四週。
目前認為造成最大有氧能力下降的因素有許多,包括血漿與血液量減少使心臟前負荷下降、心動搏出量變小、最大心輸出量降低、心臟質量縮小、骨骼肌量減少與周邊血管調控能力退化等。
最大攝氧量下降最主要的限制因素,是失重造成的最大心輸出量下降(maximal cardiac output reduction)。
而造成變化的速度也與任務時間長短密切相關:短期任務(小於 30 天)的大部分下降與血漿量減少相關,呈現較線性的型態;長期任務(可達 90 天或更久)則呈現漸近、非線性的下降趨勢,代表心臟萎縮與周邊系統的調整開始成為主要因素。
除此之外,體溫調節與乳酸堆積也是太空中運動能力降低的重要原因。
在微重力中缺乏自然對流(convection),汗液雖可分泌卻無法蒸散,使核心體溫於運動時更容易上升。
另一方面,乳酸閾值在失重下會下降,使血乳酸更容易累積,進一步加重疲勞感,也讓太空人無法像在地面上那樣維持長時間或高強度的工作與運動表現。
從預防到恢復:太空人的心血管保護策略
軌道中的運動,是太空人的「處方藥」
機上措施的目的,在於盡量減少太空人在失重環境中因心血管生理退化而導致的能力喪失,確保他們在軌道作業期間維持足夠的操作能力,也能在返回地球後具備自行離開座艙的能力。
自早期太空任務以來,運動訓練(如跑步機、划船機、腳踏車等)便始終是核心的對應措施。

在國際太空站上,太空人更使用能產生高負荷的阻力訓練設備,並將訓練頻率與強度提高,這些都比太空梭時期「每週三次」的訓練要求來得更嚴格。
儘管訓練成效會受到太空站空間限制、排班安排、個別太空人的訓練順從度等因素的影響,但從過往資料來看,結合高頻率、高強度的有氧與阻力訓練,確實能明顯減緩骨骼肌萎縮與心血管失調對生理造成的影響,使返地後姿勢不耐受的程度比沒有訓練時更輕微。
然而,即便如此,目前的運動處方仍無法完全避免 OI 的發生,相關研究也因受試者數量有限,對精準制定最佳運動策略仍有所限制。
返地前的準備:補液、加壓服、冷卻與醫療監測
返回地球是整個任務中最關鍵、也是最具挑戰性的階段之一。
太空人在失重環境中生活了一段時間後,心血管系統已經重新適應了「不需要對抗重力」的狀態,一旦降落地球,重力瞬間恢復,血液會再度往下肢傾向堆積,使本就因血漿量減少與血管收縮能力下降而變得脆弱的調節系統無法立即因應。
因此,NASA 要求太空人在著陸前後飲用約一公升含鹽的補液,以回補失重期間因利尿造成的血漿容量下降,藉此提高靜脈回流與前負荷。
太空人也會穿著反重力服,透過對腿部與腹部的外加壓力減少血液在下肢的滯留,使血壓較不會在站立時明顯下降。
另外,液體冷卻服的使用則能透過降低核心體溫,抑制因體溫上升而引起的血管擴張反應,使循環系統在重力重新出現時維持較穩定的血壓與心輸出量。
這些措施搭配地面醫療與支持團隊的監測,能協助太空人更安全地度過重新適應地球重力的過渡時期,避免在著陸後立即出現暈厥或無法站立的情形。
下一步:人造重力與下半身負壓,為太空旅行鋪路
操作能力與人員安全始終是太空飛行中最重要的考量。
如果未來太空旅行逐漸商業化,甚至朝月球與火星等更長期的任務發展,如何有效預防姿勢不耐受與心血管去條件化,便會成為必須正面面對的核心挑戰。過去幾年,科學家已開始討論並測試各種有望改善問題的策略。
例如,利用機載離心機製造人造重力,希望透過短時間、間歇性的「重力刺激」,重新訓練心血管系統維持正常的反射調節;或是透過下半身負壓裝置,模擬地球站立時下肢血液的分布,使腿部血管在太空中仍需承擔部分重力負荷,減少其功能退化。
此外,結合個人化運動處方、進階心血管監測與更高效的阻力與有氧設備,也都被認為是在長期太空任務中不可或缺的策略。
隨著這些技術逐漸成熟,也許未來的太空旅行者不再需要經歷漫長的恢復期,即使沒有接受專業太空人訓練,也能在太空中維持更穩定的心血管功能,享受一場真正「到太空、也能站得起來」的旅程。